Учебник Химии 8 Класс Рудзитис Читать
Читать книгу Химия. 8класс онлайн - автор Рудзитис Г.Е., Фельдман Ф.Г.- Химия. Неорганическая химия. Учебник для общеобразовательных. Бесплатно и без регистрации. Баг на скрепки на игру батла код на скрепки в батле коды на игру батла 3d шутер онлайн.
Новый предмет в школьной программе 8 класса - наука химия, изучающая различные вещества, их структуру и взаимодействие с другими веществами и окружающей средой. Химия только на первый взгляд кажется сложной, но, если ей заниматься так, как положено, она становится понятной и даже занимательной! Задача решебника ГДЗ в этой ситуации достаточно проста - заинтересовать и помочь. Ты найдешь в нем результаты и подробные решения отдельных заданий и целых лабораторных работ по химии, причем, в объеме за два учебных года!
Если внимательно переписывать выполненные задания в тетрадь, то решение обязательно запомнится, и в следующий раз - уже в классе - аналогичные задания в контрольных и самостоятельных работах уже не вызовут никаких затруднений.
Химия, 11 класс, Рудзитис Г.Е., Фельдман Ф.Г., 2012. Учебник для 11 класса общеобразовательных учреждений, базовый уровень. Рекомендован Министерством образования и науки Российской Федерации. В учебник включены главы 'Важнейшие химические понятия и законы', 'Периодический закон и периодическая система химических элементов Д.И. Менделеева с точки зрения учения о строении атомов', 'Строение вещества', 'Химические реакции', 'Металлы', 'Неметаллы', также содержит практические работы и ответы на задачи.
Закон сохранения массы веществ. Закон сохранения массы веществ был впервые сформулирован русским ученым М.В. Ломоносовым в 1748г. Открыл и доказал этот закон экспериментально (прокаливанием металлов в запаянных ретортах) в 1756 г.
Французский ученый А.Л. Современная формулировка закона следующая: С точки зрения атомно-молекулярной теории суть этого закона совершенно понятна.
Ведь в результате химических реакций происходит только перегруппировка атомов, т. Разрушаются связи, существующие между атомами, и образуются новые, но число атомов до и после реакции остается неизменным. Поэтому общая масса веществ в химических реакциях изменяться не должна. Ломоносов этот закон понимал гораздо глубже, о чем свидетельствует данная им формулировка: Все перемены, в натуре случающиеся, такого суть состояния, что, сколько чего у одного тела отнимается, столько присовокупляется к другому. Так, ежели где убудет несколько материи, то умножится в другом месте. Сей всеобщий естественный закон простирается и в самые правила движения, ибо тело, движущее своею силою другое, столько же оные у себя теряет, сколько сообщает другому, которое движение получает.
Из этой формулировки видно, что закон сохранения массы веществ Ломоносов рассматривал в единстве с законом сохранения энергии и понимал его как всеобщий закон природы. ОГЛАВЛЕНИЕ Как работать с учебником 3 Глава I. Важнейшие химические понятия и законы § 1. Химический элемент.
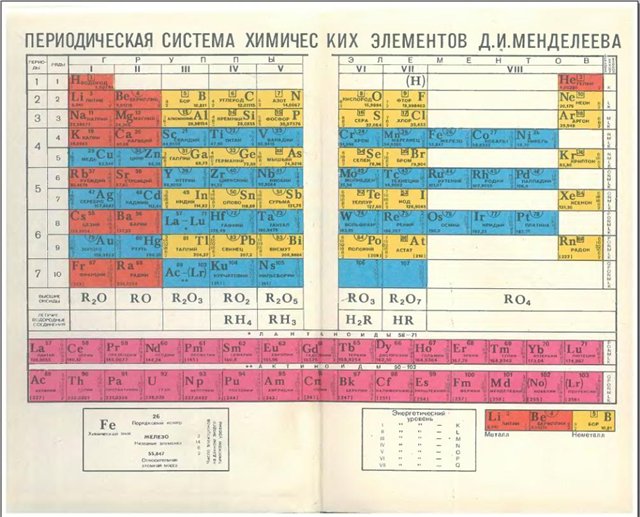
Изотопы 4 § 2. Закон сохранения массы веществ, закон сохранения и превращения энергии при химических реакциях, закон постоянства состава 5 Глава II. Периодический закон и периодическая система химических элементов Д. Менделеева с точки зрения учения о строении атомов § 3. Особенности размещения электронов в атомах малых и больших периодов. S-, p-, d-, f-Электроны 8 § 4.
Положение в периодической системе водорода, лантаноидов, актиноидов и искусственно полученных элементов 15 § 5. Валентность и валентные возможности атомов 17 Глава III. Строение вещества § 6.
Основные виды химической связи 24 § 7. Пространственное строение молекул неорганических и органических веществ 29 § 8. Типы кристаллических решеток и свойства веществ 32 § 9.
Причины многообразия веществ 34 § 10. Дисперсные системы 35 Практическая работа 1 42 Глава IV. Химические реакции § 11. Классификация химических реакций 43 § 12.
Скорость химических реакций. Катализ 49 § 13. Химическое равновесие и условия его смещения 56 § 14.
Производство серной кислоты контактным способом 58 § 15. Электролиты и неэлектролиты. Электролитическая диссоциация 63 § 16. Сильные и слабые электролиты. Степень и константа диссоциации 66 § 17. Реакции ионного обмена 68 § 18.
Гидролиз органических и неорганических соединений 70 Лабораторные опыты 75 Практическая работа 2 76 Глава V. Металлы § 19. Общие способы получения металлов. Электролиз 79 § 20.

Коррозия металлов и ее предупреждение 84 § 21. Обзор металлических элементов А-групп 89 § 22. Общий обзор металлических элементов Б-групп 98 § 23. Медь 99 § 24.
Цинк 102 § 25. Титан 104 § 26. Хром 106 § 27. Железо, никель, платина 108 § 28. Сплавы металлов 111 § 29. Оксиды и гидроксиды металлов 115 Глава VI.
Гдз По Химии
Неметаллы § 30. Обзор неметаллов 119 § 31. Оксиды неметаллов и кислородсодержащие кислоты 128 § 32. Водородные соединения неметаллов 135 § 33. Генетическая связь неорганических и органических веществ 139 § 34.
Учебник По Химии 8 Класс Рудзитис 2016 Читать Онлайн
Бытовая химическая грамотность 141 Практические работы 3—6 144 Указатель 149 Ответы на задачи 156.